Типы исследований в медицине: понятная классификация с примерами
Понимание того, какие бывают типы исследований в медицине, важно не только для научных сотрудников. С этим ежедневно сталкиваются врачи, ординаторы, аспиранты, клинические психологи, а также все, кто читает научные статьи и хочет отличать «мнение эксперта» от сильных доказательств.
В этой статье разберём:
- основные виды медицинских исследований;
- чем отличаются наблюдательные и экспериментальные исследования;
- где уместны РКИ, а где — когортное или случай–контроль;
- приведём живые примеры из практики.
1. Базовое деление: наблюдательные и экспериментальные исследования
Практически все типы исследований в медицине можно отнести к одной из двух больших групп:
- Наблюдательные исследования
- Исследователь ничего не вмешивает, а лишь наблюдает за тем, что уже происходит в реальной жизни.
- Пример: сравнение риска инфаркта у курящих и некурящих по данным регистров.
- Экспериментальные исследования (клинические испытания)
- Исследователь вмешивается: назначает новый препарат, процедуру, программу реабилитации и т.д., а затем сравнивает результаты с контрольной группой.
- Пример: рандомизированное клиническое исследование нового гипотензивного препарата.
Дальше разберём каждый вид подробнее.
2. Наблюдательные исследования в медицине
2.1. Описательные исследования
Цель: просто описать ситуацию: частоту, структуру, особенности проявления болезни или состояния.
Основные виды:
- Отчёт о клиническом случае (case report)
- Описание одного необычного пациента.
- Пример:
- Врач публикует случай редкого осложнения после стандартной операции. Это сигнал коллегам: такое бывает, будьте внимательны.
- Серия случаев (case series)
- Описание группы пациентов с общим признаком (одна болезнь, одно вмешательство).
- Пример:
- Реабилитационный центр описывает 20 пациентов после инсульта, прошедших новую программу телереабилитации, и их исходы через 3 месяца.
- Описательные популяционные исследования
- Используются для оценки распространённости (prevalence) или заболеваемости (incidence).
- Пример:
- Исследование распространённости ожирения у взрослых в определённом регионе РФ по данным диспансеризации.
Важно: описательные исследования не доказывают причинно-следственную связь, но помогают сформулировать гипотезу и понять масштаб проблемы.
2.2. Аналитические наблюдательные исследования
Здесь исследователь не вмешивается, но сравнивает группы, чтобы найти связь между фактором и исходом.
Основные типы:
2.2.1. Поперечные исследования (cross-sectional)
Что это:
Срез в один момент времени. Одновременно измеряются и фактор, и исход.
Пример:
Исследователи проводят опрос и измерения у 1000 взрослых, чтобы оценить связь между уровнем физической активности и наличием артериальной гипертензии.
Плюсы:
- относительно быстро и дёшево;
- удобно для оценки распространённости заболеваний и факторов риска.
Минусы:
- нельзя надёжно установить, что было раньше — фактор или болезнь (проблема причинности).
2.2.2. Когортные исследования
Что это:
Формируется когорта людей без исхода на старте. Сначала известно, есть ли у них фактор (например, курение). Потом за ними наблюдают во времени и фиксируют, у кого развился исход (инфаркт, инсульт, осложнение и т.д.).
Бывают:
- проспективные (наблюдение вперёд от настоящего);
- ретроспективные (анализ уже имеющихся данных, например, из истории болезни или регистра).
Пример:
Когортное исследование влияния курения на риск инфаркта:
- Когорта: 5000 человек без инфаркта на момент включения.
- Разделение: курящие и некурящие.
- Наблюдение: 10 лет.
- Исход: первый инфаркт миокарда.
Плюсы:
- хорошо подходят для оценки риска;
- можно изучать несколько исходов для одного фактора.
Минусы:
- при редких заболеваниях нужны большие выборки и длительное наблюдение;
- дороже и сложнее в организации, чем поперечные.
2.2.3. Исследования «случай–контроль» (case-control)
Что это:
Сначала выбираются случаи (люди с заболеванием), а затем подбираются контроли (люди без заболевания). Далее ретроспективно выясняют, чем группы отличались по факторам риска в прошлом.
Пример:
Редкая онкологическая патология:
- Случаи: 200 пациентов с редкой формой рака.
- Контроли: 200 человек без этого рака, сопоставимых по полу и возрасту.
- Анализ: наличие/отсутствие контакта с определённым химическим агентом в прошлом.
Плюсы:
- эффективны для редких заболеваний;
- не требуют длительного наблюдения вперёд.
Минусы:
- чувствительны к систематическим ошибкам (bias) — особенно к смещению памяти (пациенты могут по-разному вспоминать экспозицию);
- не позволяют напрямую оценить риск (обычно оценивают отношение шансов, OR).
3. Экспериментальные исследования: клинические испытания
Когда задача — оценить эффективность или безопасность нового лечения, программы реабилитации или диагностического алгоритма, используются экспериментальные (интервенционные) исследования.
3.1. Рандомизированные контролируемые исследования (РКИ)
Что это:
Участники случайным образом (рандомизация) распределяются на:
- группу вмешательства (получают новый метод, препарат, программу);
- контрольную группу (получают стандарт лечения или плацебо).
Часто применяют ослепление (blinding):
- одностороннее — пациент не знает, что получает;
- двустороннее — ни пациент, ни врач не знают;
- тройное — дополнительно не знает и аналитик.
Пример:
РКИ нового препарата для лечения артериальной гипертензии:
- 400 пациентов с АГ.
- Рандомизация: 200 человек — новый препарат, 200 — стандартная терапия.
- Наблюдение: 12 месяцев.
- Исходы: уровень артериального давления, частота сердечно-сосудистых осложнений, побочные эффекты.
Почему РКИ — «золотой стандарт»?
- Рандомизация снижает влияние смешивающих факторов.
- Контрольная группа позволяет честно сравнить эффект.
- При правильном дизайне можно делать выводы о причинно-следственной связи.
3.2. Нерандомизированные и квазиэкспериментальные исследования
Иногда рандомизация невозможна по этическим или организационным причинам.
Примеры:
- Внедрение новой программы реабилитации в одном стационаре и сравнение исходов с данными «до внедрения».
- Назначение альтернативного режима физиопроцедур пациентам, которые по каким-то причинам не подходят для стандартного лечения.
Такие исследования все равно относятся к экспериментальным, но уровень доказательности у них ниже, чем у РКИ, из-за рисков систематических ошибок.
4. Исследования диагностической точности
Отдельная важная группа — исследования диагностических тестов.
Цель: оценить, насколько хорошо новый тест или метод (анализ крови, шкала, шкрининг-опросник, МРТ-сигнал и т.п.) отличает больных от здоровых.
Ключевые показатели:
- Чувствительность — доля больных, которых тест правильно «поймал».
- Специфичность — доля здоровых, которых тест правильно «отбросил».
- Положительная и отрицательная прогностическая ценность.
- ROC-кривая и площадь под кривой (AUC).
Пример:
Оценка нового экспресс-теста на вирусную инфекцию:
- «Золотой стандарт» — ПЦР.
- Включают пациентов с подозрением на инфекцию.
- Всем делают ПЦР и новый тест.
- Сравнивают результаты и считают чувствительность/специфичность.
5. Прогностические исследования и модели риска
Цель: предсказать исход во времени (смерть, рецидив болезни, повторный инфаркт, инвалидизация после инсульта и т.д.).
Часто это:
- когортные исследования, где анализируют, какие факторы на старте предсказывают исход;
- разработка прогностической шкалы или модели риска (например, шкалы для оценки риска тромбоэмболий, шкалы для исхода инсульта и т.д.).
Пример:
Когорта пациентов с острым инсультом:
- На входе собирают данные: возраст, объём очага, NIHSS, наличие сахарного диабета и т.д.
- Через 3 месяца оценивают функциональный исход по модифицированной шкале Рэнкина.
- На основе данных строят модель, которая прогнозирует вероятность неблагоприятного исхода.
6. Систематические обзоры и мета-анализы
На вершине «пирамиды доказательств» находятся систематические обзоры и мета-анализы.
Систематический обзор — это не просто обзор литературы, а строго структурированный поиск, отбор и критическая оценка всех доступных исследований по конкретному вопросу.
Мета-анализ — статистическое объединение результатов нескольких однородных исследований, чтобы получить более точную оценку эффекта.
Пример:
- Вопрос: снижает ли телереабилитация после инсульта риск повторной госпитализации?
- Авторы ищут РКИ телереабилитации vs стандарт, отбирают 10 качественных исследований.
- Проводят мета-анализ и получают обобщённый относительный риск повторной госпитализации.
Такие работы дают самый высокий уровень доказательности, но их качество сильно зависит от включённых исследований и корректности статистического анализа.
7. Качественные исследования в медицине
Не все виды медицинских исследований основаны на цифрах. Важно изучать и субъективный опыт пациентов, врачей, родственников.
Качественные исследования используют:
- глубинные интервью;
- фокус-группы;
- наблюдение;
- анализ текстов (например, открытых ответов пациентов).
Пример:
- Интервью с пациентами после инсульта о том, что мешает им соблюдать рекомендации по домашней реабилитации.
- На основе анализа выстраиваются темы: страх, низкая мотивация, отсутствие поддержки, неудобный интерфейс приложения.
Эти данные нельзя «проанализировать t-тестом», но они критически важны при проектировании реабилитационных программ и цифровых сервисов.
8. Как выбрать тип исследования под свою задачу
Удобно ориентироваться от цели:
- Хотите описать ситуацию, частоту, структуру?
- → Описательное или поперечное исследование.
- Хотите найти возможные факторы риска?
- → Аналитическое наблюдательное: когортное или случай–контроль.
- Хотите доказать эффективность лечения/реабилитации?
- → Экспериментальное исследование, по возможности РКИ.
- Нужно оценить диагностическую ценность теста?
- → Исследование диагностической точности с расчётом чувствительности/специфичности.
- Нужно предсказывать исход (прогноз)?
- → Когорта + построение прогностической модели.
- Хотите собрать и обобщить всё, что уже есть по теме?
- → Систематический обзор (с мета-анализом или без).
При планировании важно сразу продумать:
- критерии включения/исключения;
- размер выборки (расчёт мощности);
- план статистического анализа.
9. Типы исследований и доказательная медицина
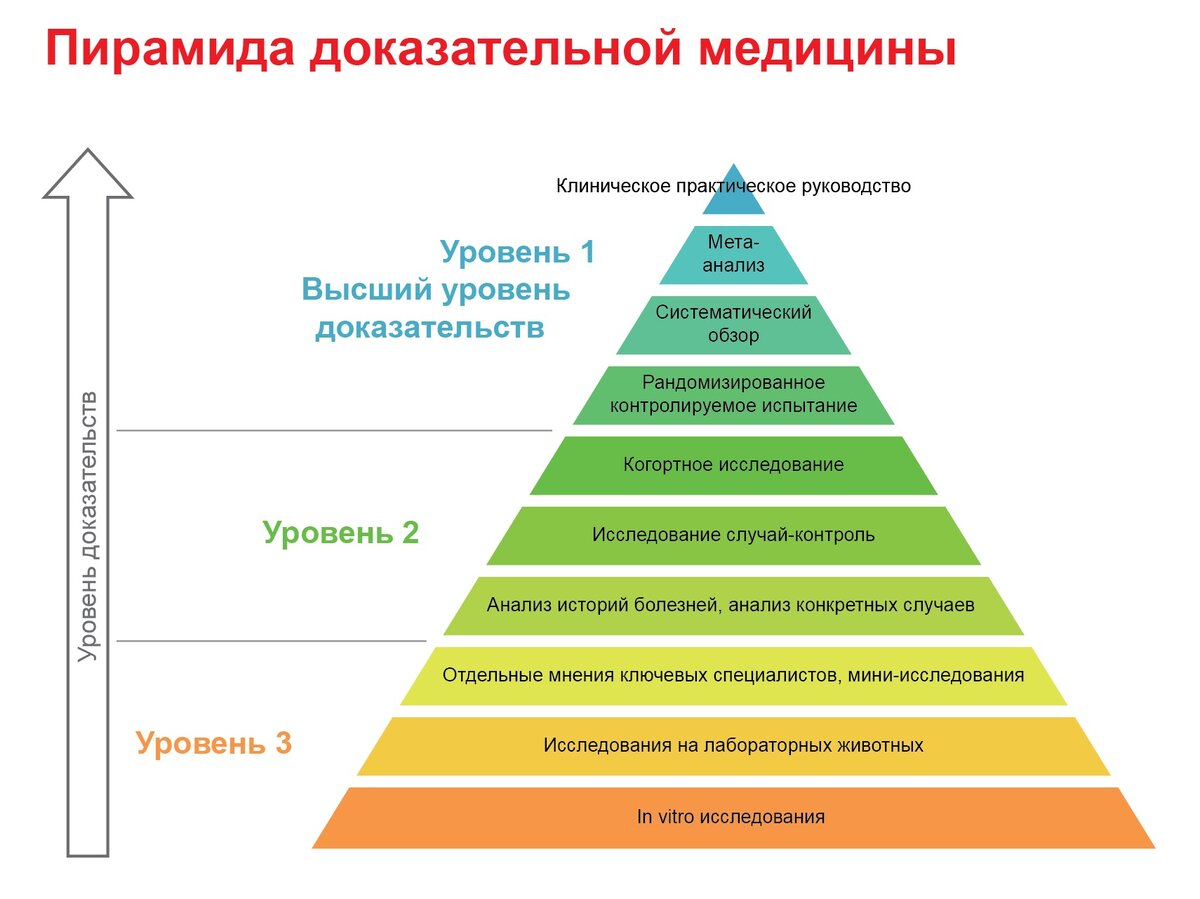
В доказательной медицине часто говорят о «пирамиде доказательств». Снизу — исследования с более низким уровнем достоверности, сверху — более надёжные:
- Мнения экспертов, описательные исследования.
- Наблюдательные аналитические исследования (когортные, случай–контроль).
- Рандомизированные клинические исследования.
- Систематические обзоры и мета-анализы РКИ.
Это не значит, что «низшие» исследования бесполезны — они часто являются единственно возможными (например, при редких заболеваниях) или стартом для формулировки гипотез.
10. Типичные ошибки при интерпретации исследований
При работе с разными типами медицинских исследований часто встречаются одни и те же ошибки:
- Путаница «корреляция = причинность»
- Из наблюдательных исследований нельзя автоматически делать вывод о причинно-следственной связи.
- Переоценка описательных данных
- Отчёт о случае не доказывает эффективность лечения, даже если исход впечатляющий.
- Игнорирование смещений и конфаундеров
- Особенно в исследованиях случай–контроль и ретроспективных когортных.
- Неправильный выбор дизайна
- Например, попытка оценить редкое заболевание в поперечном исследовании небольшой выборки.
11. Выводы
- Существует множество типов исследований в медицине, и каждый имеет свою задачу, сильные и слабые стороны.
- Ключевая развилка — наблюдательное vs экспериментальное исследование.
- Для оценки эффективности лечения лучше подходят РКИ; для факторов риска — когортные и случай–контроль; для диагностических тестов — специальные исследования точности.
- Систематические обзоры и мета-анализы дают наиболее высокий уровень доказательности, но требуют строгой методологии.
- Правильный выбор дизайна исследования и грамотный статистический анализ — критически важны для того, чтобы выводы были надёжными и действительно полезными для клинической практики.
Если вы планируете своё исследование и не уверены, какой дизайн выбрать и как посчитать объём выборки, обычно на этом этапе подключают медицинского статистика: это экономит время, деньги и помогает избежать типичных ошибок в протоколе.
Если хочешь, в следующий шаг могу:
- помочь адаптировать этот текст под структуру блога именно на med-statistic.ru (подзаголовки, внутренние ссылки);
- или сделать небольшое FAQ/блок «ошибки молодого исследователя» в конце статьи.
Вы сказали:
Перепиши этот текст используя академический и научно-популярный язык
ChatGPT сказал:
Типы исследований в медицине: систематизированный обзор с примерами
Понимание того, какие существуют типы исследований в медицине, необходимо всем, кто так или иначе работает с клиническими данными и научными статьями: врачам, ординаторам, аспирантам, клиническим психологам, научным сотрудникам. От корректного выбора дизайна исследования и адекватной интерпретации результатов напрямую зависит уровень доказательности полученных выводов.
В данной статье рассмотрены:
- основные виды медицинских исследований;
- различия между наблюдательными и экспериментальными дизайнами;
- области применения когортных и исследований «случай–контроль», рандомизированных клинических испытаний;
- примеры из клинической и реабилитационной практики.
1. Базовая классификация: наблюдательные и экспериментальные исследования
Большинство типов медицинских исследований можно отнести к одной из двух крупных категорий:
- Наблюдательные исследования
- Исследователь не вмешивается в ход событий, а лишь фиксирует уже существующую клиническую или популяционную реальность.
- Пример: анализ риска инфаркта миокарда у курящих и некурящих на основе данных регистра.
- Экспериментальные исследования (интервенционные, клинические испытания)
- Исследователь целенаправленно вмешивается: назначает новый препарат, процедуру, программу реабилитации, алгоритм ведения, а затем сравнивает результаты с контрольной группой.
- Пример: рандомизированное клиническое испытание нового антигипертензивного препарата.
Внутри этих двух направлений существует более детальная классификация, которую разберём далее.
2. Наблюдательные исследования в медицине
2.1. Описательные исследования
Цель: описание явления без формального тестирования гипотез. Оцениваются частота, структура, клинические особенности заболевания или состояния.
Ключевые формы:
- Отчёт о клиническом случае (case report)
- Детальное описание одного нестандартного или редкого клинического наблюдения.
- Пример:
- Публикация случая необычного осложнения после стандартной хирургической операции. Такой отчёт служит сигналом для клиницистов: подобное событие возможно и требует внимания.
- Серия случаев (case series)
- Описание группы пациентов с общими характеристиками (единая нозология, одинаковое вмешательство и т.п.).
- Пример:
- Реабилитационный центр описывает 20 пациентов после инсульта, прошедших новую программу телереабилитации, и фиксирует их функциональный статус через 3 месяца.
- Описательные популяционные исследования
- Направлены на оценку распространённости (prevalence) и заболеваемости (incidence).
- Пример:
- Изучение распространённости ожирения среди взрослых в конкретном регионе РФ по данным диспансеризации.
Важно: описательные исследования не позволяют делать выводы о причинно-следственных связях, но помогают формировать гипотезы и оценивать масштаб проблемы.
2.2. Аналитические наблюдательные исследования
Здесь исследователь не вмешивается в лечение, но сравнивает группы, чтобы выявить возможную ассоциацию между фактором и исходом.
2.2.1. Поперечные исследования (cross-sectional)
Сущность:
Исследование проводится в один момент времени. Фактор (экспозиция) и исход оцениваются одновременно.
Пример:
Опрос и обследование 1000 взрослых для выявления связи между уровнем физической активности и наличием артериальной гипертензии.
Преимущества:
- относительная простота и невысокая стоимость;
- возможность оценки распространённости заболеваний и факторов риска.
Ограничения:
- невозможно достоверно установить, что возникло раньше — фактор или заболевание, поэтому выводы о причинности затруднены.
2.2.2. Когортные исследования
Сущность:
Формируется когорта людей, у которых на момент включения отсутствует интересующий исход. На старте фиксируют наличие или отсутствие фактора (например, курение, ожирение, гиподинамия). Далее ведётся наблюдение во времени, регистрируется развитие исхода (инфаркт, инсульт, осложнение и др.).
Выделяют:
- проспективные когортные исследования — наблюдение «вперёд» от момента включения;
- ретроспективные — анализ уже существующих данных (истории болезни, регистры).
Пример:
Когортное исследование влияния курения на риск инфаркта:
- когорта: 5000 человек без инфаркта на момент включения;
- разделение на группы: курящие и некурящие;
- период наблюдения: 10 лет;
- исход: первый инфаркт миокарда.
Преимущества:
- позволяют рассчитывать риски (относительный риск, кумулятивный риск);
- дают возможность изучать несколько исходов для одного фактора.
Ограничения:
- при редких исходах необходимы крупные выборки и длительное наблюдение;
- высокие ресурсоёмкость и организационная сложность.
2.2.3. Исследования «случай–контроль» (case-control)
Сущность:
Сначала формируются две группы:
- случаи — пациенты с заболеванием;
- контроли — лица без этого заболевания.
Затем ретроспективно анализируется, как группы различались по фактору риска в прошлом.
Пример:
Изучение редкой онкологической патологии:
- случаи: 200 пациентов с редкой формой рака;
- контроли: 200 лиц без данного рака, сопоставимых по полу и возрасту;
- анализируется наличие/отсутствие контакта с определённым химическим агентом.
Преимущества:
- эффективны при изучении редких заболеваний;
- не требуют длительного наблюдения вперёд.
Ограничения:
- уязвимы к систематическим ошибкам (bias), особенно к смещению памяти, когда пациенты по-разному вспоминают воздействие факторов;
- не позволяют напрямую оценить риск; чаще всего рассчитывается отношение шансов (odds ratio).
3. Экспериментальные исследования: клинические испытания
При необходимости оценить эффективность и безопасность нового метода лечения, программы реабилитации, медикаментозной терапии или диагностического алгоритма используются экспериментальные (интервенционные) дизайны.
3.1. Рандомизированные контролируемые исследования (РКИ)
Сущность:
Участники случайным образом (рандомизация) распределяются на:
- группу вмешательства (получают новый метод, препарат, программу);
- контрольную группу (получают стандарт лечения либо плацебо).
Широко используется ослепление (blinding):
- одностороннее — пациент не знает, какое лечение получает;
- двустороннее — ни пациент, ни врач не знают о распределении;
- тройное — дополнительно не информирован аналитик.
Пример:
РКИ нового антигипертензивного препарата:
- 400 пациентов с артериальной гипертензией;
- рандомизация: 200 — новый препарат, 200 — стандартная терапия;
- период наблюдения: 12 месяцев;
- исходы: уровень артериального давления, частота сердечно-сосудистых осложнений, профиль безопасности (побочные эффекты).
Почему РКИ считаются «золотым стандартом»?
- рандомизация снижает влияние смешивающих факторов (confounders);
- наличие контрольной группы позволяет корректно оценить эффект вмешательства;
- при адекватном дизайне и размерe выборки РКИ дают возможность делать выводы о причинно-следственной связи.
3.2. Нерандомизированные и квазиэкспериментальные исследования
В ряде ситуаций рандомизация невозможна по этическим, организационным или юридическим причинам.
Примеры:
- внедрение новой программы медицинской реабилитации в стационаре с последующим сравнением исходов с историческим периодом «до внедрения»;
- назначение альтернативного режима физиотерапии пациентам, которые не подходят для стандартного лечения по объективным причинам.
Такие исследования относятся к экспериментальным, но уровень доказательности ниже, чем у РКИ, из-за большего риска систематических ошибок.
4. Исследования диагностической точности
Отдельная методологическая группа — исследования диагностической точности тестов.
Цель: оценка того, насколько хорошо новый диагностический тест или метод (анализ, шкала, опросник, визуализационная методика и т.п.) различает больных и здоровых.
Ключевые показатели:
- чувствительность — доля больных, которых тест корректно выявляет;
- специфичность — доля здоровых, которых тест правильно определяет как здоровых;
- положительная и отрицательная прогностическая ценность;
- ROC-кривая и площадь под кривой (AUC).
Пример:
Оценка нового экспресс-теста на вирусную инфекцию:
- «золотой стандарт» — ПЦР-диагностика;
- включаются пациенты с клиническим подозрением на инфекцию;
- всем выполняют ПЦР и новый экспресс-тест;
- результаты сравниваются, рассчитываются чувствительность, специфичность и прогностические ценности.
5. Прогностические исследования и модели риска
Цель: предсказать вероятность наступления исхода во времени (летальный исход, рецидив, повторный инфаркт, функциональный исход после инсульта и т.д.).
Как правило, используются:
- когортные исследования, в которых анализируют влияние исходных характеристик на риск события;
- разработка прогностических шкал или моделей риска (например, шкалы оценки риска тромбоэмболических осложнений, шкалы исхода при инсульте).
Пример:
Когорта пациентов с острым инсультом:
- на момент госпитализации фиксируются: возраст, неврологический дефицит (например, NIHSS), объём очага, наличие сахарного диабета и др.;
- через 3 месяца оценивается функциональный исход по модифицированной шкале Рэнкина;
- строится прогностическая модель, позволяющая оценить вероятность неблагоприятного исхода.
6. Систематические обзоры и мета-анализы
На вершине пирамиды доказательств находятся систематические обзоры и мета-анализы.
- Систематический обзор — это не просто «обзор литературы», а строго регламентированный поиск, отбор и критическая оценка всех доступных исследований по конкретному вопросу на основе заранее заданного протокола.
- Мета-анализ — статистическое объединение результатов нескольких однородных исследований с целью получить более точную интегральную оценку эффекта.
Пример:
- исследовательский вопрос: снижает ли телереабилитация после инсульта риск повторной госпитализации?
- выполняется поиск РКИ телереабилитации vs стандартная реабилитация, отбираются, допустим, 10 качественных исследований;
- проводится мета-анализ и оценивается обобщённый относительный риск повторной госпитализации.
Такие работы обеспечивают наиболее высокий уровень доказательности, однако их качество напрямую зависит от методологии поиска и качества включённых исследований.
7. Качественные исследования в медицине
Не все виды медицинских исследований опираются исключительно на количественные показатели. Для понимания опыта пациентов, их мотивации, барьеров и потребностей используются качественные исследования.
Основные методы:
- глубинные (полуструктурированные) интервью;
- фокус-группы;
- наблюдение;
- анализ текстов (например, открытых ответов пациентов в анкетах).
Пример:
- проведение серии интервью с пациентами после инсульта для выявления факторов, препятствующих соблюдению рекомендаций по домашней реабилитации;
- в результате анализа формируются темы: страх нагрузки, недостаточная мотивация, дефицит поддержки со стороны семьи, неудобный интерфейс цифрового приложения.
Подобные данные не анализируются с помощью t-теста или регрессии, но они принципиально важны при проектировании реабилитационных программ и цифровых сервисов.
8. Как сопоставить цель исследования и тип дизайна
Удобно выбирать дизайн, исходя из исследовательского вопроса:
- Нужно описать ситуацию, частоту, структуру?
- → Описательное или поперечное исследование.
- Необходимо выявить возможные факторы риска?
- → Аналитические наблюдательные исследования: когортное или «случай–контроль».
- Требуется доказать эффективность лечения или реабилитационной программы?
- → Экспериментальный дизайн, при возможности — РКИ.
- Нужно оценить диагностическую ценность теста?
- → Исследование диагностической точности с расчётом чувствительности, специфичности и ROC-анализа.
- Стоит задача прогноза исхода (прогностическая модель)?
- → Когортное исследование + построение прогностической модели.
- Важно обобщить уже накопленные данные по теме?
- → Систематический обзор с возможным мета-анализом.
При планировании исследования необходимо заранее продумать:
- критерии включения и исключения;
- размер выборки и расчёт мощности исследования;
- план статистического анализа и способы контроля смешивающих факторов.
9. Типы исследований и доказательная медицина
В рамках доказательной медицины используют концепцию «пирамиды доказательств». Условно выделяют уровни:
- Мнения экспертов, описательные исследования, отчёты о случаях.
- Наблюдательные аналитические исследования (когортные, «случай–контроль»).
- Рандомизированные контролируемые исследования.
- Систематические обзоры и мета-анализы РКИ.
Это не означает, что исследования нижних уровней «бесполезны». Во многих ситуациях (редкие заболевания, новые клинические феномены) именно они являются единственно возможным источником информации и основанием для формулировки гипотез.
10. Типичные ошибки при интерпретации результатов
При работе с различными типами медицинских исследований часто встречаются однотипные методологические ошибки:
- Отождествление корреляции и причинности
- Из наблюдательных исследований нельзя автоматически делать вывод о причинно-следственной связи.
- Переоценка описательных данных
- Отчёт о клиническом случае, даже впечатляющем, не доказывает эффективность метода лечения.
- Игнорирование систематических ошибок и смешивающих факторов
- Особенно актуально для исследований «случай–контроль» и ретроспективных когортных работ.
- Неправильный выбор дизайна
- Например, попытка изучать редкое заболевание в небольшом поперечном исследовании без достаточного объёма выборки.
11. Заключение
- Существует множество типов исследований в медицине, и каждый из них имеет свои цели, преимущества и ограничения.
- Ключевое методологическое различие — между наблюдательными и экспериментальными исследованиями.
- Для оценки эффективности вмешательства оптимальны рандомизированные контролируемые исследования; для анализа факторов риска — когортные и исследования «случай–контроль»; для оценки диагностических тестов — специальные исследования диагностической точности.
- Систематические обзоры и мета-анализы обеспечивают наиболее высокий уровень доказательности, но требуют строгого протокола и качественных исходных данных.
- Корректный выбор дизайна, расчёт объёма выборки и продуманный план статистического анализа являются критически важными условиями для получения надёжных и клинически значимых результатов.
За помощью в медицинской статистике 👉 https://med-statistic.ru/
Telegram канал 👉 https://t.me/medstatisticru
Telegram канал 👉 https://t.me/medstatisticru